Yapışma ve Birbirini Tutma

Molekülleri bir arada tutan en önemli faktör moleküller arası çekim kuvvetidir. Örneğin sıvı molekülleri arasındaki çekim kuvveti zayıf olduğundan moleküller birbirleri üzerinden kayar. Sıvı molekülleri ile diğer maddelerin molekülleri arasında da çekim kuvveti oluşur. Aynı tür moleküller arasındaki çekim kuvvetine birbirini tutma (kohezyon) kuvveti denir. Farklı tür moleküller arasındaki çekme kuvvetine yapışma (adezyon) kuvveti denir.
Adezyon ve Kohezyon Olayları

Kohezyon kuvveti sıvı moleküllerinin birbirini tutmasını sağlar. Su damlası buna örnek verilebilir. Bir su damlasını oluşturan her bir taneciğe diğer tanecikler tarafından kohezyon kuvveti uygulanır. Tanecikler öteleme hareketi yapabildikleri için kohezyon kuvveti sebebiyle birbirlerine yaklaşarak yüzey alanlarını küçültmüş olurlar. Böylelikle damlayı oluşturan tanecikler birbirlerine çok yakın şekilde toplanarak bir şekil oluşturur ve bu şekil en küçük yüzey alanına sahip olan küredir.

Adezyon kuvveti ise farklı iki madde arasındaki çekim kuvvetidir. Sıvı moleküllerinin başka yüzeylere tutunmasını sağlar. Örneğin çay tabağı ile çay bardağı arasında bir miktar su ya da çay tabakası olduğunda adezyon kuvveti sebebiyle tabak ve bardak birbirine yapışır. Adezyon kuvveti tabağın ağırlığından daha büyük olduğu için tabak bardakla birlikte hareket eder. Kontakt lenslerin göz küresinde düşmeden durabilmesinin sebebi de adezyon kuvvetidir. Gözyaşı sıvısı kontakt lensi kuvvetlice çekerek yapışmasını sağlar.
Adezyon kuvvetine yaprakta tutunan su damlası, yağmur damlalarının cama yapışması gibi birçok örnek verilebilir. Bazı durumlarda adezyon ve kohezyon kuvvetlerinden biri diğerinden büyük olabilir.
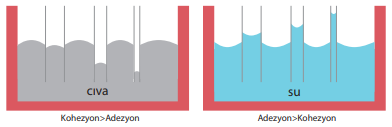
Adezyon kuvveti kohezyondan büyük olduğunda, sıvı molekülleri kabın kenarlarına daha fazla yapışacağı için içbükey şeklini alır. Kohezyon kuvveti adezyondan büyük olduğunda sıvı molekülleri arasında çekim kuvveti fazla olacağından kaptaki sıvı dışbükey şeklini alır.
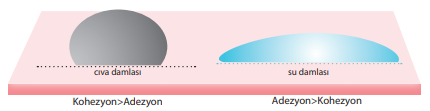
Kohezyon kuvveti adezyon kuvvetinden büyük olursa sıvı molekülleri birbirini sıkıca tutar ve sıvı yüzeye yayılamaz, bu durumda yüzey ıslanmaz. Eğer adezyon kuvveti kohezyon kuvvetinden büyükse sıvı molekülleri yüzeye daha çok tutunacağından yüzeye yayılır ve yüzey ıslanmış olur.
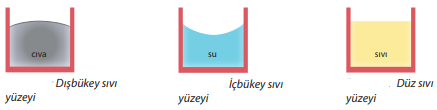
Adezyon ve kohezyon kuvvetleri sıvının, içinde bulunduğu kaptaki davranışını belirler. Kohezyon kuvveti adezyon kuvvetinden büyükse sıvı yüzeyi dışbükeydir. Adezyon kuvveti kohezyon kuvvetinden büyükse sıvı yüzeyi içbükeydir. Kohezyon kuvveti adezyon kuvvetine eşitse sıvı yüzeyi düzdür.
Yüzey gerilimi
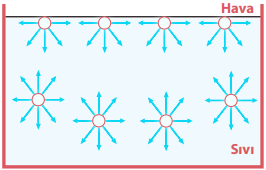
Sulu boya fırçasının tüyleri suyun içerisinde dağınık durduğu hâlde sudan çıktığında toplanmış şekildedir. Su içinde yüzerken saçlar dağınık durumdadır. Sudan çıkıldığında ise saçlar aşağıya doğru bir bütün hâldedir. Bu olaylarda sıvıların birbirine uyguladığı çekim kuvvetinin yani kohezyonun etkisi vardır. Sıvı içindeki moleküller etrafındaki diğer moleküller tarafından her yöne ortalama aynı kuvvetle çekilir.
Bu da birçok molekülün suyun içine doğru gitmesine sebep olur. Sonucunda sıvı yüzeyinde az sayıda molekül kalır. Yüzeydeki sıvı molekülleri ise sadece iç kısımdaki moleküller tarafından çekilir. Bu durum yüzeyin gergin bir zar gibi davranmasına sebep olur ve bu olaya yüzey gerilimi denir. Yüzey gerilimi katsayısının birimi SI birim sisteminde N/m veya J/m2 dir.
Yüzey gerilimi her sıvının yüzeyinde oluşan bir özelliktir. Her sıvının yüzey gerilimi aynı değildir. Yüzey geriliminin büyüklüğü; sıvının saflığına, cinsine ve sıcaklığına bağlıdır. Sıvıyı oluşturan moleküllerin cinsi yüzey geriliminde değişikliğe sebep olur. Tablo’da bazı sıvıların yüzey gerilim katsayıları gösterilmiştir.
Bir sıvının sıcaklığı arttığında kinetik enerjisi de artar. Buna bağlı olarak tanecikler daha hızlı hareket eder. Bu da tanecikler arasındaki çekim kuvvetinin azalmasına sebep olur. Çekim kuvvetinin azalmasıyla birlikte yüzeydeki taneciklerin yüzey gerilimi azalır. Örneğin suyun sıcaklığı arttıkça yüzey gerilimi azalır.
Sıvı içerisine bir başka madde eklendiğinde sıvının saflığı bozulur. Bu da yüzey gerilimini etkiler. Örneğin suyun içerisine tuz eklendiğinde suyun yüzey gerilimi artar, temizlik amaçlı kullanılan şampuan, deterjan, sabun vb. maddeler ise yüzey gerilimini azaltır. Böylelikle su molekülleri kirlere daha kolay erişir.
Ayrıca temizlik yapılırken sıcak su kullanılması daha etkili bir sonuç sağlar. Bunun sebebi suyun sıcaklığının artmasıyla yüzey geriliminin azalmasıdır. Sıvıya çözünmeyen bir başka madde eklendiğinde de yüzey gerilimi genellikle azalır. Sıvı ve madde molekülleri arasında etkileşim olacağından dolayı bu azalma meydana gelir. Bazı çözelti ve karışımlarda ise değişme gözlenmeyebilir.
- Bazı böcekler su üzerinde batmadan durabilir mi?
- Ebru sanatında su yüzeyine bırakılan boyalar su üzerinde kalabilir mi?
- Ataş ya da toplu iğne suyun üzerine yavaş şekilde bırakılırsa batar mı?
- Plastik ya da tel çerçevelerin sabunlu su ile doldurulup üflenmesi ile oluşan köpük baloncukları elde edilebilir mi?
Kılcallık
Ucu çaya dokundurulan küp şekerin çayı hızlıca çekmesi ve çayın şekeri ıslatması, gaz lambasında fitilin üst ucuna hazneden gaz yağı taşınması, spor malzemelerinde kullanılan kumaşların teri çekmesi, bitkilerde suyun köklerden yapraklara taşınması gibi olayların temelinde adezyon kuvveti etkilidir.
Sıvıların adezyon kuvvetiyle bir tüp ya da oyuk içerisinde gösterdiği yayılma hareketine kılcallık denir. Kılcallığı gözlemlemek için en pratik düzenek kılcal borulardır. İçerisinde sıvı bulunan bir cam kaba kılcal boru daldırılmasıyla oluşturulan bu düzeneklerde sıvı belli bir seviyeye kadar yükselir. Kesitleri farklı olan kılcal borularda sıvının yükselme miktarı kesit alanıyla ters orantılıdır.
Kütle (m), hacim (V) ve eylemsizliği olan her şey maddedir. Maddeler fiziksel olarak katı, sıvı veya gaz hâllerinde bulunabilir. Bir maddenin sabit sıcaklık ve basınçta kütlesiyle hacmi oranlanınca bulunan değere, o maddenin özkütlesi (d) denir. Saf maddeler karıştırılarak karışımlar elde edilir; bir karışımın özkütlesi kendini oluşturan maddelerin özkütlelerinden farklıdır.
Karışımın özkütle değeri karışanların oranları hakkında bilgi verir. Karışık hâldeki farklı özkütleli bazı sıvılar bir süre beklenince birbirinden ayrılır böylece de büyük özkütleli olanın dipte biriktiği bir ayrım gözlenir. Özkütleye dair bu bilgiler günlük yaşamda, sanatta veya endüstriyel üretimde çokça kullanılan pratik yöntemlere dönüşmüş olarak karşımıza çıkar.
Katı maddeler dış etki olmadığı takdirde sabit şekle sahiptir. Katının şeklini koruma kabiliyeti onun dayanıklılığının göstergesidir. Dayanıklılık katının kesit alanıyla doğru; hacmi ile ters orantılıdır. Sıvı moleküllerinin birbirleriyle tutunma (kohezyon) ve konuldukları kabın molekülleriyle yapışma (adezyon) kuvvetleri vardır. Bu kuvvetlerin birbirine göre miktarları sıvılara dair yüzey gerilimi, kılcallık, ıslatma gibi olaylarda belirleyicidir.
Kaynak : Fen Lisesi Fizik 9. Sınıf Ders Kitabı
Emeği Geçenler
- Abdullah AYDIN
- Ayşegül ÇELİK
- İsa YILMAZ
- Kamil SOYARSLAN
- Murat ERAT
- Şeyda BOZARSLAN



Emeği geçen herkese sonsuz teşekkürler ama ders baya zor ya